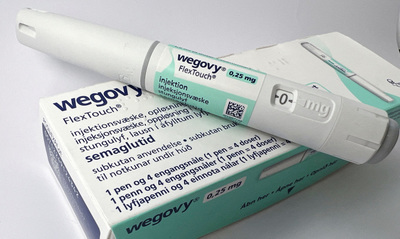
제네릭 난립·경쟁 과열·리베이트 문제까지...구조 개혁 기대감
[서울=뉴스핌] 김경민 기자 = 앞으로는 동일한 생물학적 동등성(생동성) 시험자료를 이용해 허가를 신청할 수 있는 품목이 최대 3개로 제한된다. 제약업계 구조에 큰 변화가 예상되면서 기대감도 한껏 높아졌다.
24일 식품의약품안전처(식약처)에 따르면 같은 생동성 시험자료를 활용해 허가를 신청할 수 있는 품목을 최대 3개로 제한하는 약사법 개정안이 지난 20일 공포됐다. 개정안에 따라 생동성 시험을 직접 시행한 원제조사(수탁사) 1곳당 위탁사 3곳까지 총 4곳만 제네릭 의약품 품목 허가를 받을 수 있게 된다.
 |
| [사진=게티이미지뱅크] |
생동성 시험은 복제약이 오리지널 의약품과 동일한 효과 등이 나타나는지 여부를 인체에 투여에 확인하는 시험이다. 제네릭을 허가 받기 위해선 이 생동성 시험 자료가 필요하다.
그간 국내에서는 동일한 생동성 시험 자료를 이용해 품목 허가를 신청할 수 있는 의약품의 개수에 제한이 없었다. 한 회사의 생동성 시험으로 사실상 무제한의 제네릭을 허가 받을 수 있었던 것이다.
그러나 같은 종류의 제네릭이 난립하고 이에 따른 경쟁이 과열되는 부작용을 낳았다. 특히 무차별적으로 시장이 확대되다 보니, 불법 리베이트의 주요인 중 하나로 꼽히기도 했다.
개정안이 시행되면서 제네릭 의존도가 높은 중소제약사들은 타격이 불가피할 것으로 전망된다. 하지만 업계에서는 구조 개선을 위해 필요한 수순이라며 기대감을 내비쳤다.
업계 관계자는 "중소제약사 입장에선 큰 투자 없이 제품을 만들어낼 수 있었는데, 이제 생동성 시험 등을 직접 해야 하는 변수가 생겼으니 부담이 가는 것도 사실"이라면서도 "이 회사들이 선택과 집중으로 정체성을 키울 수 있는 기회가 될 것"이라고 말했다.
또 다른 업계 관계자는 지난 2018년 고혈압 원료의약품 발사르탄에서 불순물이 검출된 일을 언급하며 "해당 성분이 함유돼 판매가 중지된 고혈압약이 영국은 5개, 미국은 10개였으나 우리나라에서는 174개나 나왔다"고 설명했다. 그러면서 "정상적인 행태는 아니다"라며 "이러한 품목 난립을 조정하는 구조적인 장치가 생긴 것"이라고도 했다.
이에 대해 한국제약바이오협회 관계자는 "이번 약사법 개정안으로 인해 동일 품목 난립에 따른 불공정 거래 등의 부작용을 해소하고, 의약품 품질관리도 더욱 강화될 것으로 기대한다"며 "협회와 산업계는 선택과 집중, 품질 혁신으로 국민들의 신뢰와 기대에 부응할 것"이라고 전했다.
kmkim@newspim.com
 영상
영상