체외진단검사 식약처 허가시 곧바로 건보 등재
[세종=뉴스핌] 임은석 기자 = 식품의약품안전처 허가부터 보험등재까지 최대 520일 걸리던 정부의 신의료기기 인허가 기간이 390일로 단축될 전망이다.
또한 올해 하반기에는 모든 체외진단검사를 대상으로 식약처 허가를 받았을 경우 곧바로 건강보험에 등재되도록 관련 절차가 통합된다.
보건복지부는 지난해 7월 발표한 '의료기기 규제혁신과 산업육성방안'의 12개 세부과제 중 8개를 완료했으며 나머지 4개 과제도 올해 안으로 마무리할 계획이다.
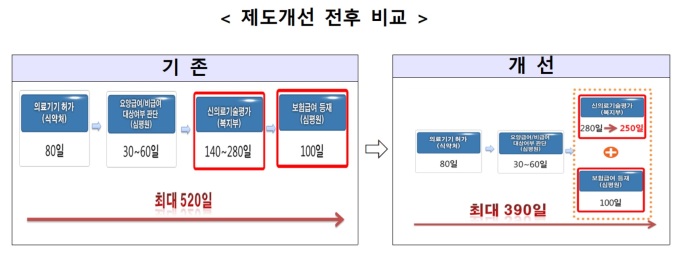
우선, 신의료기술평가 대상심의를 간소화하고 신의료기술평가와 보험등재심사를 동시에 진행한다. 지난 3월 신의료기술평가 내 불필요한 심의절차를 줄여 신의료기술평가 기간을 280일에서 250일로 30일 단축했다.
신의료기술평가와 보험등재심사를 동시에 진행해 신개발 의료기기의 보험등재까지에 기간을 이달 말까지 최대 390일로 단축할 예정이다.
오는 16일 '신의료기술평가에 관한 규칙' 입법 예고를 마친 후 법제처 심사 후 6월 말 시행할 예정이다.
또한, 의료기기 규제관련기관들이 참여하는 '의료기기산업 종합지원센터'에서 의료기긱 전 주기 통합 상담을 지원한다.
종합지원센터는 지난해부터 올해 5월까지 연구개발(R&D), 식약처 허가, 신의료기술평가, 보험등재심사 등 시장 진입 단계별 맞춤형 상담을 172개 기업 대상으로 220건 상담을 진행했으며, 전 주기 상담지원을 통해 관절꺾임 복강경 수술기 등 총 15개의 의료기기가 식약처 허가와 보험 등재 등에 성공했다.
이에 따라 올해 종합지원센터 전 주기 상담인력을 5명에서 7명으로 늘려 지난해 107건 진행된 상담 건수를 올해 250건까지 늘릴 계획이다.
'의료진의 편의와 생산성'을 증진시키는 의료기기에 대한 신의료기술평가 없이 시장에 진입이 가능하도록 예비코드도 발급할 예정이다.
복지부는 '혁신의료기술 가이드라인' 개발 등의 검토를 통해 올해 하반기에는 '건강보험 요양급여 기준에 관한 규칙' 등 관련 법령을 정비해 예비코드 발급체계를 완비한다는 방침이다.
아울러, 안전성의 우려가 적은 체외진단검사에 대해 사후 신의료기술평가 방식을 단계적으로 적용한다.
지난 4월 감염병 체외진단검사분야에 대한 선 진입·후 평가 시범사업을 실시해 건강보험 등재 신청까지의 기간을 390일에서 140일로 대폭 단축한 바 있다.
올해 하반기에는 체외진단검사 전체로 대상을 확대해 식약처 허가를 받은 체외진단검사는 곧바로 건강보험에 등재할 수 있도록 관련 절차를 통합해 기간을 390일에서 80일로 축소할 예정이다.
손호준 복지부 의료자원정책과장은 "지난 해 발표했던 '의료기기 규제혁신방안'을 조속히 추진하는 동시에, 업체들이 참여하는 '의료기기 규제혁신 협의체'를 통해 현장에서의 애로 사항을 점검할 계획"이라고 말했다.
fedor01@newspim.com























